α-羟基酮是一类非常重要的有机化合物,其常被用作光引发剂和有机合成前驱体,很多天然产物及药物分子中也包含此种结构。酮作为底物的羟基化反应是制备α-羟基酮的一类主要方法,一般利用碱来脱去α位质子,活化底物酮形成碳负离子物种,与氧气反应形成过氧化物中间体,再被三苯基膦、亚磷酸三乙酯等还原剂还原,从而得到羟基化产物(图1)。此反应通常需要金属催化剂并消耗当量的膦类化合物,因此需要开发更加绿色和环境友好的催化策略。
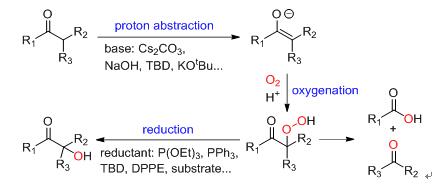
图1. 碱催化酮的氧气氧化生成α-羟基酮的反应机理。图片来源:Angew. Chem.
近日,浙江大学李浩然教授课题组在没有金属催化剂和膦还原剂的条件下,利用胍衍生物——1,5,7-三氮杂双环[4,4,0]癸-5-烯(TBD)作催化剂在DMSO中实现了酮的空气氧化,生成α-羟基酮,同时有当量的DMSO被氧化生成二甲砜 (图2)。TBD在此反应中的催化作用与其能形成双氢键的独特结构有关,其他有类似碱性的有机碱,如1,8-二氮杂二环十一碳-7-烯(DBU)、N-甲基-1,5,7-三氮杂双环[4,4,0]癸-5-烯(TBD)等,均无法催化此反应。
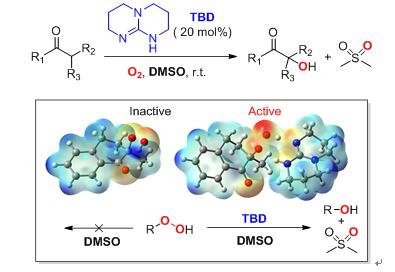
图2. TBD催化DMSO中酮的α-羟基化反应。图片来源:Angew. Chem.
作者利用条件控制实验、谱学表征、同位素动力学、量化计算等手段,对TBD在催化酮α-羟基化反应中的作用进行了深入探究,并提出反应机理(图3)。TBD不仅通过与底物形成双氢键活化酮-质子,其更为关键的作用是通过双氢键作用增强过氧化物中间体的氧化能力,使其能够氧化弱还原性的DMSO,从而不需要还原性更强的膦类化合物。氧气与烯醇式的反应是整个反应路径的决速步骤,而对过氧化物中间体的还原是决定反应选择性的关键步骤。TBD的双重催化作用不仅避免了金属催化剂的使用,而且拓展了酮羟基化反应中还原剂的选择范围。
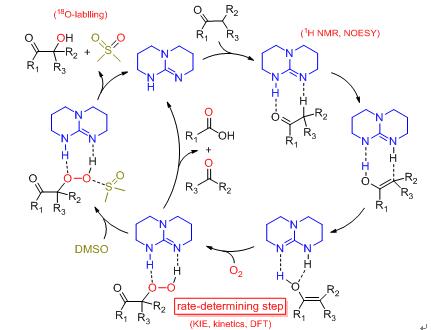
图3. TBD催化酮氧化反应的机理推测。图片来源:Angew. Chem.
此项工作为涉及过氧化物的催化氧化反应提供了一个新思路,相关成果近期发表在Angewandte Chemie International Edition上,第一作者是王永涛博士,通讯作者为李浩然教授。
论文信息:
https://onlinelibrary.wiley.com/doi/10.1002/anie.202014478
TBD‐Enhanced Activity of Peroxide Intermediates in Phosphine‐Free α‐Hydroxylation of Ketones
Yongtao Wang, Rui Lu, Jia Yao, Haoran Li
李浩然教授简介
李浩然,浙江大学化学前瞻技术研究中心执行主任。课题组主要从事绿色化学研究,尤其是空气氧化反应的工艺、机理、动力学及其催化剂、反应器设计。与同事一起先后完成了维生素E、维生素A、胡萝卜素、虾青素、紫罗兰酮、芳樟醇、柠檬醛、甲氧基丙烯等大型产业化项目,使我国维生素E、A和芳樟醇、柠檬醛系列香料居世界前列。
