通讯作者:陆展,浙江大学化学前瞻技术研究中心
作者:Tongtong Li (李同彤), Lifeng Luo (骆砺锋), Xiaokai Cheng (程骁恺), and Zhan Lu (陆展)
背景介绍
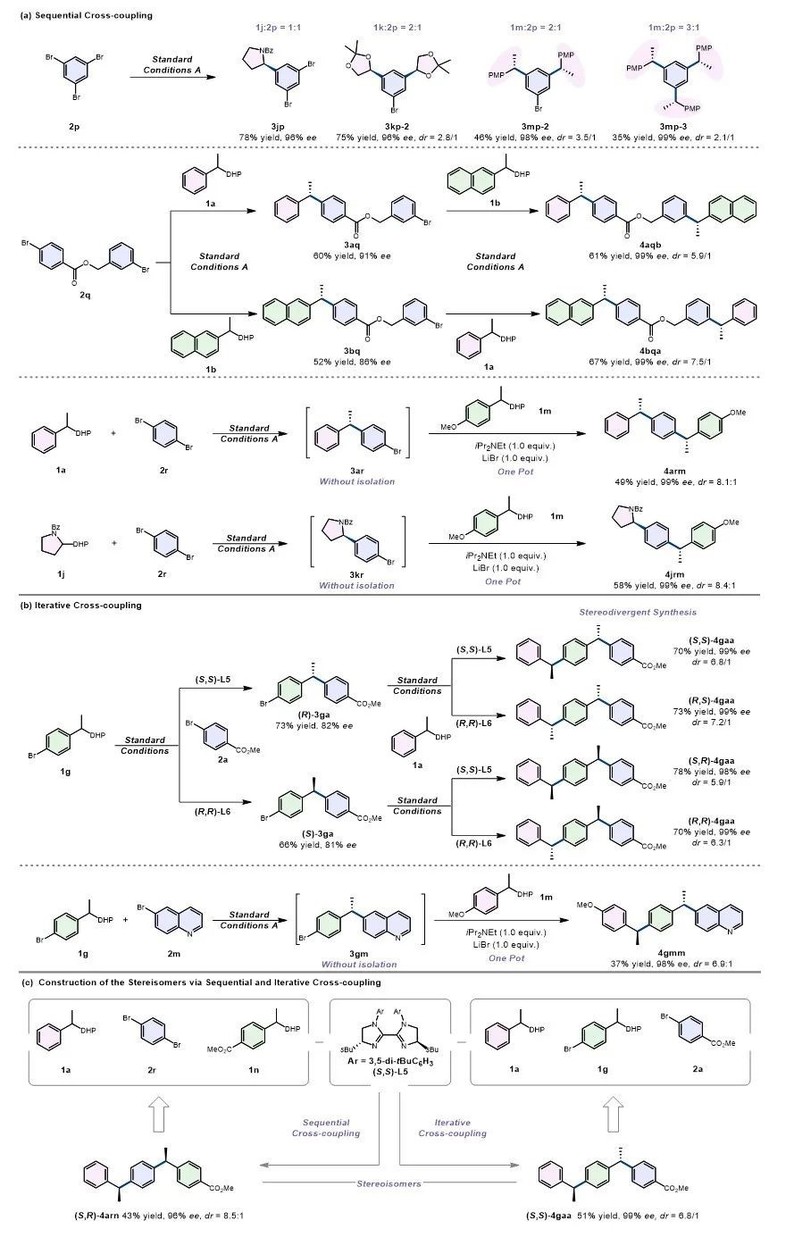
多手性中心分子广泛存在于天然产物和生物活性试剂中。在构建多手性中心的方法中,逐级迭代的策略可以构建多个碳碳键,是模块化合成以及多位点修饰的理想策略。目前一些经典的偶联方法,如Suzuki−Miyaura,Buchwald−Hartwig和Sonogashira偶联反应已经被很好的运用在逐级迭代的模型中来构建多个Csp2−Csp2,Csp2−N和Csp−Csp2键。然而利用不对称催化偶联反应通过逐级迭代来合成多个手性中心分子依然具有很大的挑战性。首先,过量的自由源或偶联试剂将会导致自身偶联以及过度偶联等副反应发生。其次,多活性位点的区域选择性,多手性中心分子的对映选择性以及非对映选择性都是需要解决的难题。因此,发展高效的不对称催化反应模式来实现逐级迭代的不对称偶联反应,合成具有高附加值的多手性中心分子非常有意义。
近日,浙江大学陆展教授团队报道了光氧化还原/镍协同催化对映汇聚式交叉偶联反应,高效高选择性得到Csp3−Csp2手性产物,反应条件温和,官能团容忍性好。该策略使用1,4-二氢吡啶衍生物(DHPs)作为自由基源和还原剂,当量的芳基/烯基卤化物作为偶联试剂,与逐级迭代策略相结合在“一锅法”中连续构建多个手性中心。动力学实验和机理研究表明,激发态光敏剂与DHPs作用生成自由基可能是反应决速步。
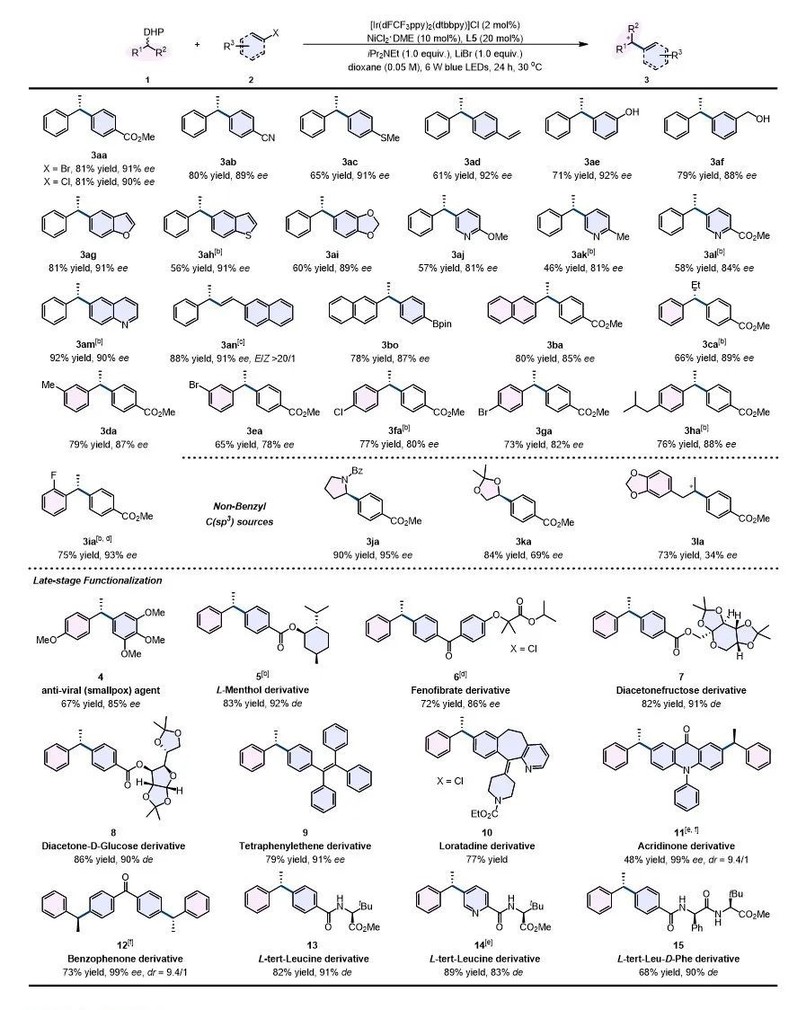
本文以[Ir(dFCF3ppy)2(dtbbpy)]Cl (2 mol %)作为光催化剂,NiCl2·DME (10 mol %)作为镍催化剂,联咪唑啉L5 (BiIm 20 mol %)作为手性配体,DIPEA(1.0当量)作为碱,当量的芳基/烯基溴化物作为偶联试剂, DHPs作为自由基源,在蓝色LED灯下,30℃反应24 h作为最优条件。条件实验表明,光催化剂,镍催化剂,碱以及光照都是反应所必须的。对底物范围进行考察(图1),酯基,氰基,甲硫基,末端烯烃,酚羟基,醇羟基,苯并呋喃,苯并噻吩,大茴香基,不同取代的吡啶,喹啉,频哪醇硼酯,卤素等基团(3aa-3gm,3bo和3ea-3ga)反应都能很好的容忍。对于非苄位自由基中间体,氮a位(3ja)和氧a位(3ka)不对称芳基化反应均能实现,而非活化的二级碳自由基中间体,也能以良好产率得到目标产物(3la)。该反应可以直接合成具有抗天花病毒活性的试剂。对薄荷醇,叔亮氨酸,葡萄糖,果糖等天然产物的衍生物,药物分子非洛贝特和氯雷他定,有机光催化剂前体吖啶酮类以及二苯甲酮化合物等复杂结构都具有很好的容忍性(4-15)。
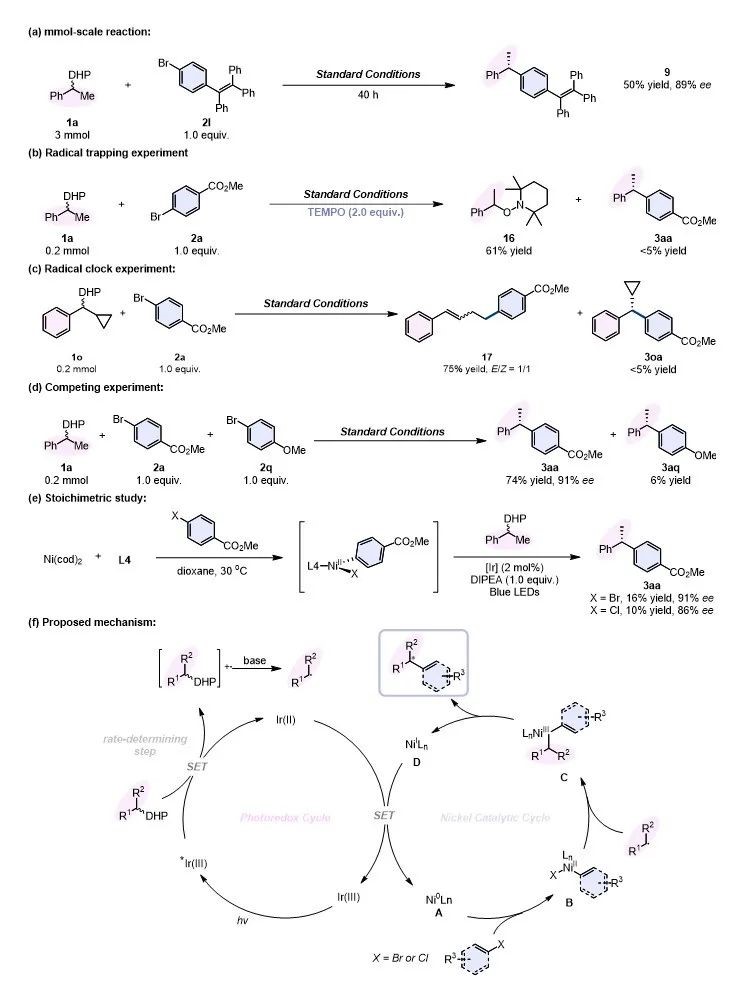
综上所述,陆展教授课题组利用光氧化还原/镍双催化体系在温和的条件下,实现了1,4-二氢吡啶衍生物(DHPs)与芳基/烯基卤化物的不对称交叉偶联反应,高效率高选择性得到Csp3-Csp2交叉偶联产物。动力学实验揭示反应的决速步可能是汉斯酯与激发态光敏剂发生单子转移的这一步。该反应官能团耐受性好,可用于多种药物分子和天然产物的合成和修饰,同时可与逐级迭代策略相结合实现多手性中心分子的高效高选择性构建。
